
Paracetamol
Antecedentes
SOS Children hizo esta selección Wikipedia junto a otros recursos de escuelas . SOS Children ha cuidado de niños en África durante cuarenta años. ¿Puedes ayudar a su trabajo en África ?
 | |
|---|---|
 | |
| Sistemático ( IUPAC ) nombre | |
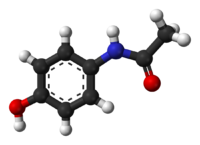
| N - (4-hidroxifenil) etanamida N - (4-hidroxifenil) acetamida | |
| Los datos clínicos | |
| Los nombres comerciales | Tylenol (EE.UU.), Anacin Aspirina gratuito (EE.UU.), Apra (EE.UU.), crocina (India), Feverall (EE.UU.), Genapap (EE.UU.), Panadol (Reino Unido), Panadol (Australia), Panodil (Dinamarca), Efferalgan (Francia ), Doliprane (Francia) Dafalgan (Francia) |
| SAIA / Drugs.com | monografía |
| MedlinePlus | a681004 |
| Datos de licencia | FDA de Estados Unidos: enlace |
| Gato Embarazo. | A ( AU ) B ( EE.UU. ) seguro |
| Estatus legal | U nscheduled ( AU ) GSL ( Reino Unido ) OTC ( Estados Unidos ) |
| Rutas | Oral, rectal, intravenoso |
| Los datos farmacocinéticos | |
| Biodisponibilidad | ~ 100% |
| Metabolismo | 90 a 95% Hepático |
| Media vida | 01.04 h |
| Excreción | Renal |
| Identificadores | |
| CAS | 103-90-2 |
| Código ATC | N02 BE01 |
| PubChem | CID 1983 |
| DrugBank | DB00316 |
| Propiedades físicas | 1906 |
| UNII | 362O9ITL9D |
| KEGG | D00217 |
| ChEBI | CHEBI: 46195 |
| ChEMBL | CHEMBL112 |
| Datos Química | |
| Fórmula | C 8 H 9 N O 2 |
| Mol. masa | 151,17 g / mol |
SONRISAS
| |
InChI
| |
| Datos físicos | |
| Densidad | 1,263 g / cm³ |
| Derrita. punto | 169 ° C (336 ° F) |
| Solubilidad en agua | 12,78 mg / ml (20 ° C) |
Paracetamol INN (pron .: / ˌ p ær ə s yo t ə m ɒ l / O / ˌ p ær ə s ɛ t ə m ɒ l /), O acetaminofeno USAN / ə ˌ s yo t ə m ɪ n ə F ɨ n /, Denomina químicamente N-acetil-p-aminofenol, es un ampliamente utilizado over-the-counter analgésico (calmante para el dolor) y antipirético (reduce fiebre).
El paracetamol se clasifica como un analgésico suave. Se utiliza comúnmente para el alivio de dolores de cabeza y otros dolores y molestias menores y es un ingrediente importante en numerosos frío y la gripe remedios. En combinación con analgésicos opioides, el paracetamol también se pueden utilizar en el tratamiento del dolor más grave tal como el dolor post-quirúrgico y proporcionar cuidados paliativos en pacientes con cáncer avanzado. Aunque el acetaminofeno se usa para tratar el dolor inflamatorio, no se clasifica generalmente como una AINE, ya que presenta sólo una débil actividad anti-inflamatoria.
El inicio de la analgesia es de aproximadamente 11 minutos después la administración oral de paracetamol, y su vida media es de 1-4 horas. Aunque generalmente seguro para su uso en las dosis recomendadas (1000 mg por dosis única y hasta 4000 mg por día para los adultos), aguda sobredosis de paracetamol pueden causar potencialmente fatal riñón, cerebro y daños en el hígado y, en raros individuos, una dosis normal puede hacer lo mismo. El riesgo puede ser mayor por crónica abuso de alcohol. La toxicidad del paracetamol es la causa más importante de insuficiencia hepática aguda en el Mundo occidental, y cuentas para la mayoría de las sobredosis de drogas en los Estados Unidos, el Reino Unido, Australia y Nueva Zelanda.
Es el metabolito activo de la alquitrán de hulla derivados fenacetina, una vez popular como analgésico y antipirético en su propio derecho. Sin embargo, a diferencia de la fenacetina y sus combinaciones, el paracetamol no se considera carcinogénico a dosis terapéuticas. El acetaminofeno palabras (utilizado en los Estados Unidos, Canadá, Japón, Corea del Sur, Hong Kong, e Irán) y paracetamol (utilizado en otros lugares), ambos vienen de un nombre químico del compuesto: para - acet il aminophen ol y un par - acet il am inophen ol. En algunos contextos, es simplemente abreviado como APAP, para una p cetyl- ara- un mino p henol.
Los usos médicos
Fiebre
El paracetamol está aprobado para reducir la fiebre en personas de todas las edades. La Organización Mundial de la Salud (OMS) recomienda que el paracetamol sólo se usa para tratar la fiebre en los niños si su temperatura es superior a 38,5 ° C (101,3 ° F). La eficacia de paracetamol por sí mismo en niños con fiebres ha sido cuestionada y un meta-análisis mostró que es menos eficaz que la ibuprofeno.
Dolor
El paracetamol se utiliza para el alivio de los dolores asociados con muchas partes del cuerpo. Tiene analgésicos propiedades comparables a las de la aspirina , mientras que sus efectos anti-inflamatorios son más débiles. Se tolera mejor que la aspirina en pacientes en los que la excesiva la secreción de ácido gástrico o la prolongación del tiempo de sangrado puede ser una preocupación. Disponible sin receta médica, lo ha hecho en los últimos años cada vez más se convierten en un fármaco común de la casa.
El paracetamol puede aliviar el dolor en la artritis leve, pero no tiene ningún efecto sobre la inflamación subyacente, enrojecimiento e hinchazón de la articulación. Es tan eficaz como el no esteroideo antiinflamatorio ( NSAID) ibuprofeno para aliviar el dolor de la osteoartritis de la rodilla.
Paracetamol tiene relativamente poca actividad anti-inflamatoria, a diferencia de otros analgésicos comunes, tales como la AINE aspirina y el ibuprofeno.
Respecto comparativo eficacia, los estudios muestran resultados contradictorios cuando se compara con los AINE. La ensayo controlado aleatorio de dolor crónico de osteoartritis en adultos encontró beneficio similar de paracetamol y el ibuprofeno.
La eficacia del paracetamol cuando se utiliza en una forma combinación con opioides débiles (por ejemplo, codeína) ha sido cuestionada por los estudios de datos recientes; la pequeña cantidad de datos disponibles han hecho llegar a una conclusión difícil. Drogas de combinación de paracetamol y opioides fuertes como la morfina se ha demostrado para reducir la cantidad de opiáceo usado y mejorar efecto analgésico, así como el uso excesivo de los opiáceos adictivos desalentador debido a los efectos tóxicos de APAP, ya que agota el glutatión y de este modo exacerba la enfermedad en general.
Un ensayo controlado aleatorio de dolor musculoesquelético agudo en niños encontró que la dosis estándar over-the-counter de ibuprofeno da un mayor alivio del dolor que la dosis estándar de paracetamol.
Efectos adversos
En las dosis recomendadas, la efectos secundarios del paracetamol son leves o inexistentes. En contraste a la aspirina, que no es una antitrombótica, y por lo tanto se pueden usar en pacientes en los que coagulación es una preocupación, y que no causa irritación gástrica. Sin embargo, el paracetamol no ayuda a reducir la inflamación, mientras que la aspirina hace. En comparación con ibuprofeno cuyos efectos secundarios pueden incluir diarrea, vómitos y dolor abdominal-paracetamol tiene menos efectos adversos gastrointestinales. El uso diario prolongado aumenta el riesgo de complicaciones gastrointestinales superiores como sangrado en el estómago, y puede causar daño a los riñones o el hígado. El paracetamol se metaboliza por el hígado y es hepatotóxicos; los efectos secundarios pueden ser más probable en alcohólicos crónicos o pacientes con daño hepático.
Hasta 2010, el paracetamol se creía segura en el embarazo (ya que no afecta el cierre de la fetal ductus arterioso como los AINE pueden). Sin embargo, en un estudio publicado en octubre de 2010 que se ha relacionado con infertilidad en la vida adulta de los no nacidos. A diferencia de la aspirina, es seguro para los niños, como el paracetamol no se asocia con un riesgo de El síndrome de Reye en los niños con enfermedades virales. El uso de paracetamol para la fiebre en el primer año de vida se asoció con un aumento en la incidencia de asma síntomas a los 6-7 años, y que el uso de paracetamol, tanto en el primer año de vida y en los niños de 6-7 años, se asoció con una mayor incidencia de rinoconjuntivitis y eccema . Los autores reconocieron que sus "hallazgos podrían haber sido debido a la confusión por indicación", es decir, que la asociación no sea causal, sino más bien debido a la enfermedad que está siendo tratado con paracetamol, e hicieron hincapié en que se necesita más investigación. Por otra parte, una serie de editoriales, comentarios, correspondencia y sus respuestas han sido publicados en la revista The Lancet sobre la metodología y las conclusiones de este estudio. El organismo regulador del Reino Unido el Medicamentos y Productos Sanitarios, también revisaron esta investigación y se publicaron una serie de preocupaciones sobre la interpretación de los datos, y ofrecen los siguientes consejos para profesionales de la salud, padres y cuidadores: "Los resultados de este nuevo estudio no requieren ningún cambio la orientación actual para su uso en niños. El paracetamol sigue siendo una opción segura y adecuada de analgésico en los niños. No hay suficiente evidencia de esta investigación para cambiar la orientación sobre el uso de antipiréticos en niños. "
Los usuarios crónicos de paracetamol pueden tener un mayor riesgo de desarrollar cáncer de la sangre.
Sobredosis
Hepatotoxicidad Paracetamol es, con mucho, la causa más común de insuficiencia hepática aguda, tanto en Estados Unidos y el Reino Unido. Toxicidad de paracetamol surge a menudo debido a su metabolito quinona. Resultados por sobredosis de paracetamol en más llamadas a los centros de toxicología en los EE.UU. que la sobredosis de cualquier otra sustancia farmacológica. Los signos y síntomas de la toxicidad del paracetamol inicialmente pueden estar ausentes o vaga. Sobredosis no tratada puede conducir a la insuficiencia hepática y la muerte en pocos días. El tratamiento está encaminado a eliminar el paracetamol del cuerpo y su sustitución glutatión. El carbón activado se puede utilizar para disminuir la absorción de paracetamol si el paciente presenta para el tratamiento poco después de la sobredosis. Mientras que el antídoto, acetilcisteína, (también llamado N-acetilcisteína o NAC) actúa como un precursor para el glutatión, ayudando al cuerpo regenerar suficiente para evitar daños en el hígado, una trasplante de hígado a menudo se requiere si el daño al hígado se convierte en grave. N-acetilcisteína también ayuda a neutralizar el metabolito imidoquinone de acetaminofeno. La insuficiencia renal es también un posible efecto secundario.
Hay tabletas disponibles (de marca en el Reino Unido Paradote) que combinan el paracetamol con un antídoto ( metionina), para proteger el hígado en el caso de una sobredosis.
En junio de 2009, un Administración de Alimentos y Medicamentos (FDA) comité asesor recomienda que las nuevas restricciones se deben colocar sobre el uso de paracetamol en los Estados Unidos para ayudar a proteger a las personas de los efectos tóxicos potenciales. La dosis máxima en un momento dado se redujo de 1,000 mg a 650 mg, mientras que las combinaciones de paracetamol y narcóticos analgésicos estarían prohibidas. Los miembros del comité estaban especialmente preocupados por el hecho de que se habían demostrado las actuales dosis máximas de paracetamol para producir alteraciones en la función hepática. El 13 de enero de 2011, la FDA pidió a los fabricantes de productos combinados con receta que contienen paracetamol para limitar la cantidad de paracetamol a no más de 325 mg por comprimido o cápsula y comenzó a exigir a los fabricantes a actualizar las etiquetas de todos los productos combinados con receta paracetamol para advertir de la el riesgo potencial de daño hepático grave. Los fabricantes tendrán tres años para limitar la cantidad de paracetamol en sus productos de medicamentos recetados a 325 mg por unidad de dosificación. En noviembre de 2011, el Medicamentos y Productos Sanitarios Agencia Reguladora revisó UK dosis de paracetamol líquido para los niños.
Clasificación
El paracetamol es parte de la clase de medicamentos conocidos como " analgésicos anilina ";.. que es la única droga todavía en uso hoy en día, no se considera un AINE, ya que no presenta actividad antiinflamatoria significativa (es un inhibidor de la COX débil) Esto es a pesar de la evidencia de que el paracetamol y AINE tienen alguna actividad farmacológica similar.
Mecanismo de acción

Hasta la fecha, el mecanismo de acción del paracetamol no se entiende completamente. El principal mecanismo propuesto es la inhibición de la ciclooxigenasa (COX), y los hallazgos recientes sugieren que es altamente selectivo para COX-2. Mientras que tiene analgésico y propiedades antipiréticas comparables a las de la aspirina u otro AINE, su actividad anti-inflamatoria periférica es generalmente limitada por varios factores, uno de los cuales es el alto nivel de peróxidos presentes en lesiones inflamatorias. Sin embargo, en algunas circunstancias, la actividad anti-inflamatoria periférica incluso comparable a Los AINE pueden ser observados. Un artículo publicado en Nature Communications de investigadores en Londres, Reino Unido y Lund, Suecia en noviembre de 2011 ha encontrado una pista para el mecanismo analgésico del paracetamol (acetaminofeno), siendo que los metabolitos del paracetamol por ejemplo, NAPQI, actuar en TRPA1-receptores en la médula espinal para suprimir la transducción de señales de las capas superficiales del asta dorsal, para aliviar el dolor. Esta conclusión ha sido impugnada en un nuevo documento de hipótesis sobre cómo podría actuar paracetamol. El autor reconoce que NAPQI es el metabolito activo pero que este compuesto reactivo debe reaccionar no sólo con el tiol en TRPA1 sino también con cualquier otro nucleófilo convenientemente disponibles que pasa a encontrar. Se sugiere que los grupos tiol en cisteína proteasas, por ejemplo, las proteasas que participan en el procesamiento de procytokines, tales como los de generación IL-1β y IL-6, podrían ser los objetivos que dieron lugar a efectos analgésicos en general.
Debido a su selectividad por la COX-2 no inhibe significativamente la producción de la pro-coagulación tromboxanos.
La familia de la COX de las enzimas son responsables para el metabolismo de ácido araquidónico a prostaglandina H 2, una molécula inestable que es, a su vez, convierte a numerosos otros compuestos pro-inflamatorias. Antiinflamatorios clásicos como la AINE bloquean este paso. Sólo cuando se oxida apropiada es la enzima COX altamente activa.
El paracetamol reduce la forma oxidada de la enzima COX, evitando que se formen productos químicos pro-inflamatorias. Esto lleva a una cantidad reducida de prostaglandina E2 en el SNC, reduciendo así el punto de ajuste hipotalámico en el centro termorregulador.
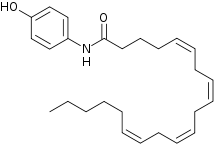
Paracetamol también modula la sistema cannabinoide endógeno. El paracetamol se metaboliza a AM404, un compuesto con varias acciones; lo que es más importante es que inhibe la recaptación de la endógeno cannabinoide / vaniloide anandamida por las neuronas. La recaptación de anandamida se traduciría en niveles sinápticos más bajos y menos activación del receptor de dolor principal (nociceptores) del cuerpo, la TRPV1 (antiguo nombre: vanilloid receptor). Mediante la inhibición de la recaptación de anandamida, los niveles en la sinapsis siguen siendo elevadas y son capaces de desensibilizar el receptor TRPV1 como mucho capsaicina. Además, AM404 inhibe los canales de sodio, al igual que la lidocaína y procaína anestésicos. Cualquiera de estas acciones por sí mismos se ha demostrado para reducir el dolor, y son un posible mecanismo para el paracetamol. Sin embargo, se ha demostrado que, después de bloquear los receptores de cannabinoides con antagonistas sintéticos, se evitan efectos analgésicos de paracetamol, lo que sugiere su acción de alivio del dolor implica el sistema cannabinoide endógeno. Espinal Receptores TRPA1 también se han demostrado para mediar los efectos antinociceptivos de paracetamol y Δ9-tetrahydrocannabiorcol en ratones.
La aspirina es conocida para inhibir la ciclooxigenasa (COX), la familia de enzimas y, debido a la acción del paracetamol es parcialmente similar a la aspirina de muchas investigaciones se ha centrado en si el paracetamol también inhibe la COX. Ahora está claro que el paracetamol actúa a través de al menos dos vías.
Los mecanismos exactos por los que la COX se inhibe en diversas circunstancias siguen siendo un tema de discusión. Debido a las diferencias en la actividad de paracetamol, aspirina y otros AINE, se ha postulado que pueden existir otras variantes de la COX. Una teoría sostiene que el paracetamol actúa inhibiendo la Isoforma COX-3 - un inhibidor de COX-1 empalme variante - de la familia de enzimas de COX. Cuando se expresa en los perros, esta enzima comparte una fuerte similitud con las otras enzimas COX, produce productos químicos pro-inflamatorias, y se inhibe selectivamente por paracetamol. Sin embargo, algunas investigaciones han sugerido que, en humanos y ratones, la enzima COX-3 es sin acción inflamatoria y bloqueo de paracetamol de él no es significativa en su funcionamiento en humanos. Otra posibilidad es que los bloques de paracetamol ciclooxigenasa (como la aspirina), pero que, en un ambiente inflamatorio donde la concentración de peróxidos es alta, el alto estado de oxidación del paracetamol impide sus acciones. Esta idea que significaría que el paracetamol no tiene ningún efecto directo en el sitio de la inflamación, pero en su lugar actúa en el SNC donde el medio ambiente no es oxidativo, para reducir la temperatura, etc. El mecanismo exacto por el cual se cree paracetamol para afectar a la COX-3 se discute .
Estructura y reactividad

El paracetamol se compone de un benceno núcleo anular, sustituido por uno grupo hidroxilo y el nitrógeno de un átomo grupo amida en el párrafo (1,4) patrón. El grupo amida es acetamida (etanamida). Es un extensivamente sistema conjugado, como el par solitario sobre el oxígeno hidroxilo, la nube pi benceno, el par solitario del nitrógeno, el p orbital en el carbono del carbonilo, y el par solitario en el oxígeno del carbonilo están conjugados. La presencia de dos grupos de activación también hacen que el anillo de benceno altamente reactivo hacia sustitución electrofílica aromática. Como los sustituyentes son orto, -directing para y para con respecto a la otra, todas las posiciones en el anillo son más o menos igualmente activado. La conjugación también reduce en gran medida la basicidad de los oxígenos y el nitrógeno, al tiempo que el hidroxilo ácida a través de la deslocalización de la carga desarrollada en el fenóxido de aniones .
Síntesis
En el laboratorio, el paracetamol se prepara fácilmente por nitración de fenol con nitrato de sodio, separar el apartado nitrofenol deseado de la orto - subproducto, y la reducción de la grupo nitro con borohidruro de sodio. La resultante 4 aminofenol se acetila luego con anhídrido acético. En esta reacción, el fenol está activando fuertemente, por lo que la reacción requiere sólo condiciones suaves (cf. la nitración del benceno). El proceso industrial es análogo, pero hidrogenación se utiliza en lugar de la reducción con borohidruro de sodio.
Una síntesis más simple por Hoechst-Celanese implica acilación directa del fenol con anhídrido acético catalizada por HF, la conversión de la cetona a una cetoxima con hidroxilamina, seguido por el ácido-catalizada Transposición de Beckmann para dar la amida.
La demanda de paracetamol en los Estados Unidos se estimó en 30 a 35.000 toneladas por año en 1997, igual a la demanda del resto del mundo.
Metabolismo

Paracetamol es metaboliza principalmente en el hígado, en productos tóxicos y no tóxicos. Tres vías metabólicas son notables:
- La glucuronidación se cree que representan el 40% a los dos tercios del metabolismo del paracetamol.
- La sulfatación (conjugación sulfato) puede dar cuenta de 20-40%.
- N-hidroxilación y reordenamiento, entonces GSH conjugación, representan menos del 15%. El hepática sistema enzimático citocromo P450 metaboliza paracetamol, formando un menor metabolito alquilante pero significativo conocido como NAPQI (N -acetil- p-benzo-quinona imina) (también conocido como N-acetylimidoquinone). NAPQI es entonces irreversiblemente conjugado con el grupos sulfhidrilo de glutatión.
Los tres vías producen productos finales que están inactivas, no tóxico, y, finalmente excretado por los riñones. En la tercera vía, sin embargo, el NAPQI producto intermedio es tóxico. NAPQI es principalmente responsable de los efectos tóxicos del paracetamol; esto constituye un ejemplo de intoxicación.
Producción de NAPQI se debe principalmente a dos isoenzimas del citocromo P450: CYP2E1 y CYP1A2. El gen P450 es altamente polimórfica, sin embargo, y las diferencias individuales en la toxicidad del paracetamol se cree que debido a la tercera isoenzima, CYP2D6. Polimorfismos genéticos en CYP2D6 puede contribuir significativamente a diferentes tasas de producción de NAPQI. Además, los individuos pueden ser clasificados como "amplias", "ultrarrápidos", "intermedias" y metabolizadores "pobres" (productores de NAPQI), en función de sus niveles de expresión de CYP2D6. Aunque CYP2D6 metaboliza paracetamol en NAPQI en menor medida que otros enzimas P450, su actividad puede contribuir a la toxicidad del paracetamol en los metabolizadores extensos y ultrarrápidos, y cuando el paracetamol se toma en dosis muy grandes. A dosis habituales, NAPQI se desintoxica rápidamente por conjugación con glutatión. Después de la sobredosis, y posiblemente también en los metabolizadores extensos y ultrarrápidos, esta vía de desintoxicación se satura, y, como consecuencia, NAPQI acumula causando toxicidad hepática y renal.
Reacciones
4 aminofenol se puede obtener la amida hidrólisis de paracetamol. 4 -aminofenol preparado de esta forma, y en relación con la disponible en el mercado Metol, se ha utilizado como desarrollador en la fotografía por los aficionados. Esta reacción también se utiliza para determinar paracetamol en muestras de orina: Después de la hidrólisis con ácido clorhídrico, 4 aminofenol reacciona en una solución de amoníaco con un derivado de fenol, por ejemplo, ácido salicílico, para formar una indofenol teñir bajo oxidación por aire.
Historia

Acetanilida fue el primero derivado de anilina casualmente encontrado que poseen analgésico, así como propiedades antipiréticas, y se introdujo rápidamente en la práctica médica bajo el nombre de Antifebrin por A. Cahn y P. Hepp en 1886. Pero sus efectos tóxicos inaceptables, siendo el más alarmante cianosis debido a metahemoglobinemia, impulsado la búsqueda de derivados de anilina menos tóxicos. Harmon Northrop Morse ya había sintetizado en paracetamol Universidad Johns Hopkins a través de la reducción de p-nitrofenol con estaño en glacial ácido acético en 1877, pero no fue hasta 1887 que farmacólogo clínico Joseph von Mering intentó paracetamol en pacientes. En 1893, von Mering publicó un artículo que informa sobre los resultados clínicos de paracetamol con fenacetina, otro derivado de anilina. Von Mering afirmado que, a diferencia de la fenacetina, paracetamol tuvo una ligera tendencia a producir metahemoglobinemia. Entonces Paracetamol fue rápidamente descartada en favor de fenacetina. Las ventas de fenacetina establecieron Bayer como una compañía farmacéutica líder. Eclipsado en parte por la aspirina , introducido en la medicina por Heinrich Dreser en 1899, fenacetina fue popular durante muchas décadas, sobre todo en ampliamente publicitados over-the-counter "mezclas de dolor de cabeza", por lo general contienen fenacetina, un derivado aminopirina de la aspirina, la cafeína, ya veces un barbitúricos.
Reclamaciones de Von Mering se mantuvo esencialmente sin respuesta durante medio siglo, hasta que dos equipos de investigadores de Estados Unidos analizaron el metabolismo de acetanilida y paracetamol. En 1947 David Lester y León Greenberg encontraron pruebas sólidas de que el paracetamol fue un metabolito principal de la acetanilida en la sangre humana, y en un estudio posterior se informó que grandes dosis de paracetamol dadas a ratas albinas no causaron metahemoglobinemia. En tres artículos publicados en la edición de septiembre 1948 de la Revista de Farmacología y Terapéutica Experimental, Bernard Brodie, Julius Axelrod y Frederick Flinn confirmaron el uso de métodos más específicos que el paracetamol fue el principal metabolito de la acetanilida en la sangre humana, y establecieron que era igual de eficaz analgésico como su precursor. También sugirieron que la metahemoglobinemia se produce en los seres humanos principalmente por otro metabolito, fenilhidroxilamina. Un documento de seguimiento por Brodie y Axelrod en 1949 estableció que la fenacetina también se metaboliza a paracetamol. Esto condujo a un "redescubrimiento" de paracetamol. Se ha sugerido que la contaminación de paracetamol con 4-aminofenol, la sustancia von Mering sintetiza desde, puede ser la causa de sus hallazgos espurios.
El paracetamol se comercializó por primera vez en los Estados Unidos en 1953 por Sterling Winthrop-Co, que lo promovió como preferible a la aspirina ya que era seguro tomar para los niños y las personas con úlceras. El más conocido de marca hoy para paracetamol en los Estados Unidos, Tylenol, se estableció en 1955, cuando McNeil Laboratories comenzó a vender el paracetamol como un calmante para el dolor y la fiebre de los niños, bajo el nombre de marca de Tylenol Niños Elixir-la palabra "Tylenol" era una contracción del párrafo -Ace tyl aminoph enol. En 1956, 500 mg comprimidos de paracetamol salieron a la venta en el Reino Unido bajo el nombre comercial Panadol, producido por Frederick Stearns & Co, subsidiaria de la Sterling Drug Inc. Panadol estuvo disponible inicialmente sólo con receta médica, para el alivio del dolor y la fiebre, y se anuncia como "suave para el estómago", ya que otros agentes analgésicos de la época contenían aspirina, un irritante estomacal conocido. En 1963, el paracetamol se añadió a la Farmacopea Británica, y ha ganado popularidad desde entonces como un agente analgésico con pocos efectos secundarios y poca interacción con otros agentes farmacéuticos. Las preocupaciones sobre la seguridad del paracetamol retrasaron su aceptación generalizada hasta la década de 1970, pero en la década de 1980 las ventas de paracetamol fueron superiores a los de la aspirina en muchos países, incluido el Reino Unido. Esto fue acompañado por la desaparición comercial de fenacetina, culpó como la causa de nefropatía por analgésicos y la toxicidad hematológica.
Los EE.UU. patente sobre el paracetamol ha vencido hace tiempo, y las versiones genéricas de la droga están ampliamente disponibles en el marco del Precios de Medicamentos Competencia y Ley de Restauración de duración de la patente de 1984, a pesar de ciertos preparados de Tylenol estaban protegidos hasta el 2007. La patente US 6.126.967, presentada el 3 de septiembre, fue otorgado a "Extended partículas de acetaminofeno de liberación" de 1998.
Formas disponibles


Paracetamol está disponible en una tableta, cápsula, suspensión líquida, supositorio, intravenosa, y intramuscular. La dosis para adultos común es 500 mg a 1.000 mg. La dosis diaria máxima recomendada, para los adultos, es de 4000 mg. En las dosis recomendadas, el paracetamol es generalmente seguro para los niños y bebés, así como para los adultos, aunque raros casos de lesión hepática aguda se han relacionado con importes inferiores a 2.500 mg por día.
Panadol, que se comercializa en África, Asia, Europa, América Central, y Australasia, es la marca de mayor disponibilidad de paracetamol, que se vende en más de 80 países. En América del Norte, el paracetamol se vende en forma genérica (generalmente etiquetado como acetaminofeno) o bajo una serie de nombres comerciales, por ejemplo, Tylenol ( McNeil-PPC, Inc.), Anacin-3, Tempra, Datril y Ofirmev. Si bien no es de marca llamado paracetamol disponible en el Reino Unido (por ejemplo, Panadol), paracetamol sin marca o genérico se vende más comúnmente. Acamol, un nombre de marca para el paracetamol producido por Teva Pharmaceutical Industries de Israel , es uno de los fármacos más utilizados en ese país. En Filipinas, la marca de paracetamol de mayor venta es Biogesic, fabricado por el gigante farmacéutico United Laboratories. Las ventas de tabletas Biogesic alcanzan casi mil millones de unidades cada año en el país por sí solo, sin incluir formatos suspensión líquida. La marca también está disponible en la mayor parte del Países de la ASEAN en el que el gigante farmacéutico tiene presencia en el mercado. En Europa, las marcas más comunes de paracetamol son Efferalgan y Doliprane. En la India, la marca más común de paracetamol se crocina fabricado por Glaxo SmithKline Asia. En Bangladesh, el más popular de dos marcas son Napa y Renova fabricado por Beximco Pharma y opsoninas Pharma respectivamente. En China el paracetamol se vende sin receta médica como Duìyǐxiān'ānjīfēn Pian (对乙酰氨基酚片). Del mismo modo que en Japón se vende bajo el nombre de El acetaminofeno (アセトアミノフェンAsetoaminofen). En Corea del Norte, la empresa conjunta y la RPDC suizo PyongSu Pharma comercializa la droga como PyongSu Cetamol.
En algunas formulaciones, el paracetamol se combina con el opioide codeína, a veces conocido como co-codamol ( BAN). En los Estados Unidos y Canadá, este se comercializa bajo el nombre de Tylenol # 1/2/3/4, que contiene 8-10 mg, 15 mg, 30 mg, y 60 mg de codeína, respectivamente. En los EE.UU., esta combinación está disponible sólo con receta médica, mientras que la preparación de menor fuerza es over-the-counter en Canadá, y, en otros países, otras fuerzas pueden estar disponibles en el mostrador. Hay formas genéricas de estas combinaciones también. En el Reino Unido y en muchos otros países, esta combinación se comercializa bajo los nombres de Tylex CD y Panadeine. Otros nombres incluyen Captin, Disprol, Dymadon, Fensum, Hedex, Mexalen, Nofedol, Panocod, Paralen, Pediapirin, Perfalgan y Solpadeine. Paracetamol también se combina con otros opioides tales como dihidrocodeína, denominado co-dydramol ( BAN), oxicodona o hidrocodona, comercializado en los EE.UU. como Percocet y Vicodin, respectivamente. Otra combinación analgésica muy comúnmente usado incluye paracetamol en combinación con napsilato propoxifeno, vendido bajo el nombre de marca Darvocet. Una combinación de paracetamol, codeína, y la calmative succinato de doxilamina se comercializa como Syndol o Mersyndol. La eficacia de la combinación de paracetamol / codeína ha sido cuestionada por la investigación reciente.
El paracetamol se utiliza comúnmente en preparaciones múltiples ingredientes para dolor de cabeza de migraña, que incluye típicamente butalbital y paracetamol con o sin cafeína , y algunas veces contienen codeína.
El uso veterinario
El paracetamol es extremadamente tóxico para los gatos, que carecen de la necesaria enzimas transferasa glucuronilo para romper con seguridad hacia abajo. Los síntomas iniciales incluyen vómitos, salivación, y decoloración de la lengua y las encías. A diferencia de una sobredosis en humanos, daño hepático rara vez es la causa de la muerte; en su lugar, la formación de metahemoglobina y la producción de Cuerpos de Heinz en las células rojas de la sangre inhiben el transporte de oxígeno por la sangre, causando asfixia ( methemoglobemia y anemia hemolítica). El tratamiento con N-acetilcisteína, azul de metileno o ambos es a veces eficaz después de la ingestión de pequeñas dosis de paracetamol.
Aunque se cree que el paracetamol no tener actividad anti-inflamatoria significativa, se ha informado de tan eficaz como la aspirina en el tratamiento del dolor musculoesquelético en perros. Un producto paracetamol codeína (nombre comercial Pardale-V) con licencia para su uso en perros está disponible bajo prescripción veterinaria en el Reino Unido. Se debe administrar a los perros sólo en asesoramiento veterinario y con extrema precaución. El principal efecto de toxicidad en los perros es el daño hepático, ulceración GI ha sido reportado. Tratamiento con N-acetilcisteína es eficaz en los perros cuando se administra dentro de las 2 horas de la ingestión de paracetamol.
Paracetamol también es letal para las serpientes, y se ha sugerido como un programa de control químico para la invasivo marrón de árbol serpiente (Boiga irregularis) en Guam . Las dosis de 80 mg se insertan en ratones muertos dispersos en helicóptero.


